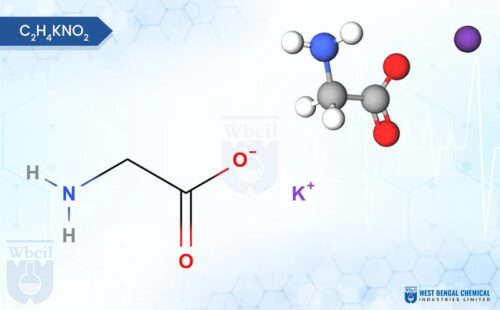
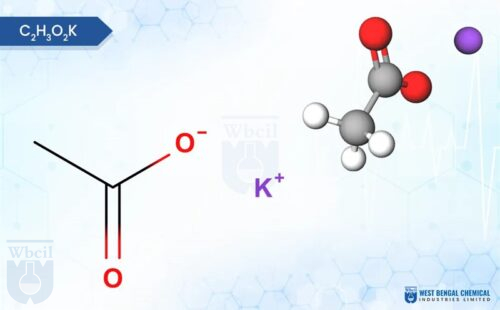
Toepassingen van kaliumacetaat: een strategische keuze voor actieve farmaceutische ingrediënten (API’s) als alternatief voor chloride
Kaliumacetaat is een van die verbindingen die geruisloos de meest kritische processen in de moderne wetenschap, geneeskunde en industrie aandrijft, maar zelden de aandacht krijgt die het verdient. Van het stabiliseren van infuusvloeistoffen op de intensive care tot het conserveren van gekoelde visproducten en het bufferen van cosmetische formuleringen; het functionele bereik is indrukwekkend breed.
Werkt u in de farmaceutische industrie, levensmiddelenproductie, landbouw of moleculaire biologie? Dan helpt een diepgaand begrip van deze verbinding u bij het maken van onderbouwde beslissingen op het gebied van inkoop, formulering en toepassing.
Ontdek de technische specificaties en farmaceutische standaarden van onze Kaliumacetaat API.
Belangrijkste inzichten:
- Metabole alkalisering: Kaliumacetaat onderscheidt zich klinisch van kaliumchloride bij gebruik in infusen en TPN (totale parenterale voeding).
- Veiligheid in voeding: Als additief (E261) kent het geen numerieke ADI (aanvaardbare dagelijkse inname), wat duidt op een uitstekend veiligheidsprofiel.
- Landbouwvoordeel: Het presteert beter dan kaliumchloride bij chloridegevoelige gewassen zonder de bodem op lange termijn te verzuren.
Kort samengevat: Kaliumacetaat is een veelzijdig kaliumzout dat essentieel is voor infuusvloeistoffen, voedselconservering (E261), pH-buffering in cosmetica, DNA-extractieprotocollen en landbouwvoeding.

Kaliumacetaat in de Farmaceutische Industrie: Kernwaarden van de API
De toepassingen van kaliumacetaat bepalen de formuleringsstrategieën binnen uw wereldwijde farmaceutische toeleveringsketen. Dit zout fungeert als een cruciaal actief farmaceutisch ingrediënt (API).
Dit zijn de belangrijkste parameters voor kaliumacetaat als API:
- Behandeling van Hypokaliëmie: Klinische protocollen vereisen deze verbinding om ernstige kaliumtekorten te corrigeren. U formuleert dit doorgaans in een standaardconcentratie van 2 mEq/mL voor intraveneuze therapieën.
- Exacte Moleculaire Massa: De zuivere verbinding heeft een exact molecuulgewicht van $98,14 \text{ g/mol}$. Dankzij deze specifieke massa lost het zout snel op, wat essentieel is voor heldere vloeibare medicatie.
- Correctie van Acidose: Het acetaat-ion werkt als een alkaliserend middel in het menselijk lichaam [1]. Dit mechanisme stelt u in staat om metabole acidose te corrigeren zonder de patiënt bloot te stellen aan een overmaat aan chloriden.[1]
- Totale Parenterale Voeding (TPN): TPN vereist een nauwkeurige mineralenbalans wanneer patiënten geen vast voedsel kunnen consumeren. U voegt deze zuivere chemische stof toe aan de vloeistoffen om de elektrolytenspiegels exact te beheersen.
- pH-Stabilisatie: Deze heldere oplossingen vereisen een strikte naleving van farmacopee-normen tussen pH 5,5 en 8,0. U vertrouwt op deze verbinding om die zuurgraad stabiel te houden.
Nu we de farmaceutische basis begrijpen, kijken we naar het cruciale verschil tussen kaliumacetaat en kaliumchloride.
Kaliumacetaat vs. Kaliumchloride in Infuusvloeistoffen
Kaliumacetaat en kaliumchloride zijn beide intraveneuze kaliumvervangende middelen die worden gebruikt om hypokaliëmie te corrigeren. Ze verschillen echter aanzienlijk wat betreft hun metabolische effecten, klinische indicaties en compatibiliteitsprofielen.
Hieronder volgt een tabel om het verschil tussen beide middelen te verduidelijken:
| Parameter | Kaliumacetaat | Kaliumchloride |
| Metabool effect | Acetaat wordt omgezet in bicarbonaat, wat een licht alkaliserende werking heeft | Een hoge chloridebelasting kan bijdragen aan hyperchloremische acidose |
| Voornaamste indicatie | Er is sprake van hypokaliëmie in combinatie met metabole acidose of een beperkte chloride-inname | Standaardbehandeling van hypokaliëmie; hypokaliëmische metabole alkalose |
| Voorkeur in TPN | Ja, wordt vaak gebruikt bij parenterale voeding om de Cl⁻-belasting te beperken | Minder geprefereerd bij TPN; wordt wel gebruikt, maar kaliumacetaat heeft de voorkeur |
| Belangrijkste klinische overweging | De voorkeur gaat uit naar dit middel wanneer een beperking van het chloridegehalte noodzakelijk is (bijv. hyperchloremie, renale tubulaire acidose) | Eerste keuze in de meeste klinische situaties; corrigeert hypokaliëmie in combinatie met hypochloremie of alkalose |
Naast essentiële medische toepassingen wordt kaliumacetaat ook op veelzijdige wijze gebruikt om commerciële voedingsmiddelen te stabiliseren en cosmetische formules te conserveren.
Toepassingen in Voeding en Cosmetica
Kaliumacetaat fungeert als een pH-verlagend conserveermiddel in bewerkte voedingsmiddelen zoals sauzen, soepen en snacks. Het remt de groei van bacteriën, gisten en schimmels door een omgeving te creëren die ongunstig is voor microbiële activiteit.
De EFSA bevestigt dat er geen numerieke ADI nodig is, aangezien acetaatzouten snel worden gemetaboliseerd en zich niet ophopen in het lichaam.
1. Natriumreductie en Formulering van Natriumarme Voeding
Kaliumacetaat dient als natriumvrij alternatief voor natriumacetaat en natriumdiacetaat. Het biedt vergelijkbare antimicrobiële effecten zonder de natriuminname te verhogen. Hiermee is E261 een essentieel instrument voor fabrikanten die willen voldoen aan de wereldwijde richtlijnen van de WHO voor natriumreductie.
2. Antimicrobiële Effectiviteit in Vis en Vlees
Onderzoek toont aan dat de combinatie van kaliumacetaat en kaliumlactaat de houdbaarheid van gekoelde visfilets aanzienlijk verlengt [2]. Behandelde producten vertoonden lagere bacteriële counts na 7 tot 14 dagen opslag bij 4°C.
3. pH-Buffering in Cosmetische Formuleringen
In persoonlijke verzorgingsproducten stabiliseert kaliumacetaat de pH-waarde, zodat deze compatibel blijft met de natuurlijke zuurmantel van de huid. Gezien het feit dat veel cosmetische preparaten nog steeds een te hoge pH-waarde hebben, is het gebruik van een effectieve buffer cruciaal voor barrièrebeschermende producten [3].
4. Ondersteuning van de Huidbarrière
Een zure huid-pH reguleert de homeostase van het stratum corneum en de huidmicrobiotica. Studies tonen aan dat emulsies met een pH van 4 superieur zijn aan die met een pH van 5,8 voor hydratatie en herstel van de lipidenlaag [4]. De buffercapaciteit van kaliumacetaat maakt het een functioneel ingrediënt voor geavanceerde huidverzorging.
Lees ook: Biopharma SHAKTI-initiatief: waarom WBCIL het voortouw neemt in deze transitie

Gespecialiseerd Gebruik: DNA-extractie en Landbouw
Kaliumacetaat vervult cruciale, gespecialiseerde functies die verder reiken dan de voedings- en geneeskundige sector; het wordt gebruikt als precisie-reagens bij DNA-extractieprotocollen in de moleculaire biologie en als multifunctioneel landbouwmiddel dat van invloed is op de bodemchemie, de gewasfysiologie en de microbiële ecologie.
Hier volgen twee toepassingen van kaliumacetaat die u moet kennen:
DNA-extractie
- Eiwitprecipitatie: Bij de ‘alkaline lysis’-methode voor plasmide-DNA-extractie precipiteert kaliumacetaat gedenatureerde eiwitten en genomisch DNA.
- Optimale concentratie: Een oplossing met een pH van 4,8 (meestal 3M of 5M) is de standaard in het bekende Birnboim-Doly protocol.
- Selectiviteitsmechanisme: Het acetaat-ion verlaagt de pH abrupt, waardoor plasmide-DNA herstelt terwijl chromosomaal DNA en eiwitten samenklonteren tot een wit neerslag.
Landbouw
- Voeding voor chloridegevoelige gewassen: Onmisbaar voor gewassen zoals tabak, avocado en citrusvruchten, waarbij kaliumchloride bladverbranding en toxiciteit kan veroorzaken.
- Neutrale bodem-pH: In tegenstelling tot kaliumchloride, dat bodems kan verzuren, laten micro-organismen na de afbraak van acetaat een neutraal tot licht alkalisch effect achter.
- Efficiënte bladopname: Via bladvoeding wordt kaliumacetaat efficiënter opgenomen dan ionische zouten, omdat acetaat de membraanpermeabiliteit bevordert.
Lees ook: Hoe WBCIL nieuwe merken ondersteunt bij het ontwikkelen van farmaceutische formuleringen op maat.
Inkoop van Kaliumacetaat bij een Bulk API-leverancier
Het selecteren van een leverancier voor kaliumacetaat vereist een kritische evaluatie van productiecertificaten, naleving van regelgeving en betrouwbaarheid van de leveringsketen. WBCIL (West Bengal Chemical Industries Limited) is een gevestigde speler die GMP-conforme productie biedt. Onze materialen voldoen aan de IP/BP/USP-specificaties van de farmaceutische industrie, inclusief volledige traceerbaarheid van grondstof tot eindproduct.
Bij bulkinkoop moet u parameters zoals zuiverheid (assay), limieten voor zware metalen, pH-bereik en watergehalte verifiëren via het analysecertificaat (CoA). Daarnaast zijn leveranciersaudits en ondersteuning bij registraties doorslaggevend voor uw succes.
Conclusie
Een diepgaand inzicht in de toepassingen van kaliumacetaat stelt professionals in de farma, voedingswetenschap en landbouw in staat om veiligere en slimmere keuzes te maken. Controleer altijd de relevante farmacopee-specificaties voor uw specifieke toepassing. Voor farmaceutische bulktoepassingen maakt een samenwerking met een GMP-conforme fabrikant zoals WBCIL het verschil in productkwaliteit.
- PubChem. Potassium acetate. [online] pubchem.ncbi..
- Kin, S., Schilling, M.W., Smith, B.S., Silva, J.L., Kim, T., Pham, A.J. and Campano, S.G. (2011). Potassium Acetate and Potassium Lactate Enhance the Microbiological and Physical Properties of Marinated Catfish Fillets. Journal of Food Science, 76(4), pp.S242–S250.
- Wohlrab, J. and Gebert, A. (2018). pH and Buffer Capacity of Topical Formulations. pH of the Skin: Issues and Challenges, [online] 54, pp.123–131.
- Kilić, A., Masur, C., Reich, H., Knie, U., Dorothee Dähnhardt, Dähnhardt‐Pfeiffer, S. and Abels, C. (2019). Skin acidification with a water‐in‐oil emulsion (pH 4) restores disrupted epidermal barrier and improves structure of lipid lamellae in the elderly. The Journal of Dermatology, 46(6), pp.457–465.
Kaliumacetaat is een verbinding met een opmerkelijk breed toepassingsgebied, dat zich uitstrekt van de klinische geneeskunde tot de levensmiddelentechnologie, cosmetica, moleculaire biologie en landbouwkunde. Zijn functionele veelzijdigheid is te danken aan de ionische dissociatie in K⁺ en acetaat⁻, die elk in verschillende systemen een eigen biologische en chemische werking hebben.
Het cruciale verschil zit hem in het anion: acetaat is metabolisch actief en heeft een alkaliserende werking, terwijl chloride vanuit zuur-base-oogpunt fysiologisch inert is. De keuze tussen beide is dus een klinische beslissing die wordt bepaald door de zuur-base-balans van de patiënt, en niet alleen door zijn of haar kaliumtekort.
Wereldwijd beoordelen regelgevende instanties levensmiddelenadditieven aan de hand van een gelaagd veiligheidsspectrum, en kaliumacetaat bevindt zich aan de gunstigste kant daarvan, waarbij geen kwantitatieve innamebeperking noodzakelijk wordt geacht. De metabolische verwerking ervan is identiek aan die van natuurlijk voorkomend acetaat in het lichaam, wat het gunstige toxicologische profiel ervan sterk onderbouwt.
De werking ervan is puur fysisch-chemisch; het maakt gebruik van het verschil in renaturatiegedrag tussen plasmide-DNA en chromosomaal DNA onder zure omstandigheden om een selectieve scheiding te bewerkstelligen. Geen enkel ander gangbaar reagens weet deze combinatie van een scherpe pH-daling en ionische neerslag in één enkele toevoegingsstap te evenaren.
Deze voorkeur is gebaseerd op de plantenfysiologie; sommige gewassen hebben genetisch bepaalde lage tolerantiedrempels voor chloride, die door kaliumchloride steevast worden overschreden, ongeacht de dosering. Kaliumacetaat omzeilt dit probleem volledig door kalium aan te voeren via een anion dat het bodemecosysteem op natuurlijke wijze verwerkt, waardoor er geen fytotoxische residuen achterblijven.